Pour comprendre l'eau hydrogénée, il faut déjà commencer par les bases, c'est-à-dire :
 Qu'est-ce-que l'hydrogène, hydrogène moléculaire, le dihydrogène ou hydrogène diatomique ?
Qu'est-ce-que l'hydrogène, hydrogène moléculaire, le dihydrogène ou hydrogène diatomique ?
L'hydrogène est l'élément le plus léger et le plus simple avec le symbole H. Il se compose d'un seul électron et un proton et , dans des conditions normales, il existe principalement sous sa forme diatomique, dihydrogène ( H2 gazeux ) . Il est ce qui alimente le soleil par fusion pour produire de l'hélium.
L'hydrogène est le centre du modèle cosmologique dominant qui décrit le développement précoce de l'Univers ainsi que l'origine de la vie elle- même.
Il est considéré comme le père de tous les éléments . Il est le premier élément sur la table de Mendeleïev et également présent en nous sous la forme H20 (eau). Il est la plus petite particule dans l'univers, et cette très petite taille et sa solubilité élevée en lipides permet de diffuser facilement dans les compartiments subcellulaires des mitochondries et d'autres locations.
 Forme de l'atome d'hydrogène
Forme de l'atome d'hydrogène
Un atome d'hydrogène seul (H •) est neutre et a un électron non apparié (représenté par le petit point "•" ). Il est donc d'un radical libre réactif, ce qui est la raison pour laquelle l'hydrogène atomique est rare. Lorsque de l'hydrogène atomique est produit par électrolyse, il réagit facilement avec un autre atome d'hydrogène pour former de l'hydrogène moléculaire stable (H • • H + -> H2).
Dans les années 1990, il a été suggéré que l'hydrogène atomique était responsable des effets thérapeutiques de ERW3. Cet hydrogène atomique réactif a probablement été mal traduit du japonais à l'anglais comme " hydrogène actif " 3 ; cependant, le terme " hydrogène actif " est pas un terme scientifique et est fréquemment utilisé dans battage marketing pseudo- scientifique. En outre, l'existence stable de l'hydrogène atomique dans des solutions aqueuses reste à prouver, 4 et à partir d'un point de vue de la chimie physique impossible. L'hydrogène atomique est le premier élément dans l'existence et le premier élément du tableau périodique ; il peut être considéré comme le père de tous les éléments.
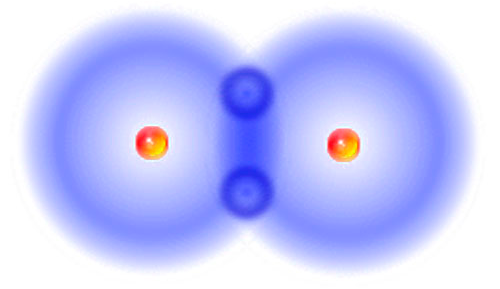 La molécule d'hydrogène, dihydrogène, hydrogène moléculaire ou H2, antioxydant puissant et sélectif à la fois
La molécule d'hydrogène, dihydrogène, hydrogène moléculaire ou H2, antioxydant puissant et sélectif à la fois
La molécule d’hydrogène ou H2 appelée aussi diatomique ou dihydrogène est la principale forme dans laquelle l'hydrogène se trouve. En d'autres termes, deux atomes d'hydrogène (H) sont liés de manière covalente (un type de liaison chimique), ainsi que H-H. Parce qu'il y a deux atomes d'hydrogène, nous appelons cet hydrogène diatomique, di signifie deux. Etant donné que les atomes d'hydrogène sont liés de manière covalente ensemble, ils forment une molécule.
La molécule d'hydrogène contient deux protons et deux électrons qui en font une molécule neutre chargée. Il est, inodore, insipide, non métallique gaz hautement inflammable incolore et très explosif au-dessus d'une concentration de 4,6% en volume. Certains articles se réfèrent à ce que "l'eau riche en hydrogène" exerce une large gamme d'effets thérapeutiques.
 Hydrure : l'anion hydrogène
Hydrure : l'anion hydrogène
L'hydrure est un atome d'hydrogène, qui a un électron supplémentaire. Il a un proton et deux électrons, ce qui en fait un ion négatif écrit H- . Étant donné que l'atome d'hydrogène a reçu un électron supplémentaire, il ne dispose pas d'un électron non apparié et est donc plus un radical libre. Cependant, il n’est toujours pas stable parce que, dans cette forme, il est une base très solide. En tant que tel, il va réagir avec l'eau pour produire de l'hydrogène moléculaire (H + H2O -> H2 + OH- 6. La plupart des hydrures sont des composés chimiques (par exemple le borohydrure de sodium, l' hydrure de lithium aluminium , etc.) utilisés comme agent réducteur dans la synthèse chimique .
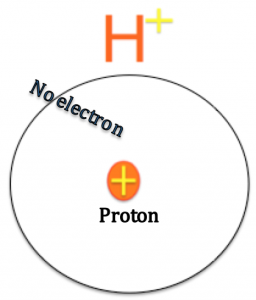 Le cation d’hydrogène (H+) : Acide ou alcalin
Le cation d’hydrogène (H+) : Acide ou alcalin
Un ion hydrogène chargé positivement (cation ou H+) est également connu comme un simple proton. Parce qu'un atome d'hydrogène n'a qu'un seul électron et d'un proton. Si l'atome perd son électron, il est seulement un proton.
Il est présent sous forme d'hydrogène qui entraîne l'enzyme ATP synthase dans les mitochondries. Les mitochondries sont considérées comme la " puissance " de la cellule car elle produit la majorité de l'ATP (adénosine triphosphate), qui est la monnaie de l'énergie de nos cellules.
L'ion hydrogène (H +) est ce qui est responsable du pH de l'eau (i.e. acide ou alcaline). L'eau se dissocie pour former des protons (H +) et hydroxydes (OH-). C'est : H2O ⇆ H + + OH- . Ceci est appelé " auto- ionisation " de l'eau.
Le pH est le log de l'ion hydrogène de concentration (H +). Ainsi, plus les ions H+ sont présent plus le pH de l’eau est acide.
Source :
- OHNO, K., ITO, M. & ICHIHARA, M. (2012). Molecular hydrogen as an emerging therapeutic medical gas for neurodegenerative and other diseases. Oxidative Medicine and Cellular Longevity 2012, 353152.
- BLACK, J. H. (2006). Chemistry and cosmology. Faraday Discussions 133, 27-32; discussion 83-102, 449-52.
- SHIRAHATA, S., KABAYAMA, S., NAKANO, M., MIURA, T., KUSUMOTO, K., GOTOH, M., HAYASHI, H., OTSUBO, K., MORISAWA, S. & KATAKURA, Y. (1997). Electrolyzed-reduced water scavenges active oxygen species and protects DNA from oxidative damage. Biochemical and Biophysical Research Communications 234, 269-274.
- HIRAOKA, A., TAKEMOTO, M., SUZUKI, T., SHINOHARA, A., CHIBA, M., SHIRAO, M. & YOSHIMURA, Y. (2004). Studies on the properties and real existence of aqueous solution systems that are assumed to have antioxidant activities by the action of "active hydrogen"'. Journal of Health Science 50, 456-465.
- OHTA, S. (2012). Molecular hydrogen is a novel antioxidant to efficiently reduce oxidative stress with potential for the improvement of mitochondrial diseases. Biochimica et Biophysica Acta 1820, 586-94.
- <>http://pubchem.ncbi.nlm.nih.gov/summary/summary.cgi?cid=166653</>
- <>Harris, D. C. (2010). Quantitative chemical analysis. Macmillan. 8th ed. p 127</>
Traduction du site http://www.molecularhydrogenfoundation.org/
